Fedtceller omprogrammeres til øget fedtforbrænding
Kroppens hvide fedtvæv oplagrer overskydende kalorier som fedtdepoter, hvorimod brunt fedtvæv, som mennesker kun har meget lidt af, primært virker som en effektiv fedtforbrænder. Nu har forskere fra Syddansk Universitet afdækket den mekanisme, der bruner de hvide fedtceller fra mennesker og sætter forbrændingen i vejret.
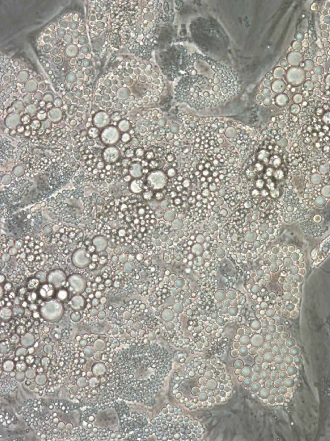 Bruning af hvidt fedtvæv øger kroppens energiforbrug og er derfor et potentielt middel i fremtidens behandling af fedme. Udfordringen består i at omprogrammere de energi-lagrende hvide fedtceller til såkaldte ”brite” (brown-in-white) fedtceller i kroppens hvide fedtvæv og dermed få fedtvævet til at forbrænde overskydende energi som varme i stedet for at lagre det.
Bruning af hvidt fedtvæv øger kroppens energiforbrug og er derfor et potentielt middel i fremtidens behandling af fedme. Udfordringen består i at omprogrammere de energi-lagrende hvide fedtceller til såkaldte ”brite” (brown-in-white) fedtceller i kroppens hvide fedtvæv og dermed få fedtvævet til at forbrænde overskydende energi som varme i stedet for at lagre det.
Forskergruppen fra Institut for Biokemi og Molekylær Biologi med professor Susanne Mandrup i spidsen beskriver deres resultater af arbejdet med ”brite” fedtceller i en forskningsartikel med titlen ”Browning of human adipocytes requires KLF11 and reprogramming of PPARγ super-enhancers” i januar-udgaven af det videnskabelige tidsskrift ”Genes & Development”.
”Vi har undersøgt, hvordan det er muligt at brune de hvide fedtceller og fundet ud af, hvordan cellens genom omprogrammeres, når hvide fedtceller udvikler sig til ”brite” fedtceller. Ved at benytte hvide fedtceller fra mennesker, som er blevet brunet ved hjælp af diabetesmedicin, har vi kunnet sammenligne hvide og ”brite” fedtceller og fundet frem til, at ”brite” fedtcellerne har nogle særlige genprogrammer, som, når de er aktive, gør cellen særligt energiforbrugende,” siger Susanne Mandrup og fortsætter:
”Ved at identificere de områder i genomet, som er direkte involveret i omprogrammeringen, har vi samtidig identificeret en vigtig faktor i processen – det gen-regulerende protein KLF11 (Kruppel Like Factor-11), som findes i alle fedtceller, og som er nødvendig for, at omprogrammeringen kan finde sted.”
En af de absolutte hovedkræfter bag projektet og førsteforfatter til forskningsartiklen er ph.d.-studerende Anne Loft, der er meget glad for resultaterne.
”Det har været en lang proces og har taget fire år at nå hertil, så det er selvfølgelig meget tilfredsstillende, når resultaterne er så brugbare, som det er tilfældet her," siger Anne Loft og peger på de fremtidige perspektiver af forskningen i ”brite” fedtceller.
”Fundet af ”brite” fedtcellernes mekanismer og særlige regulatoriske områder bringer os tættere på at forstå, hvordan omprogrammeringen af de hvide fedtceller foregår. Den viden betyder potentielt, at vi i fremtiden kan målrette medicin til at aktivere de genomiske områder og bruningsfaktorer som KLF11 i behandlingen af fedme,” slutter Anne Loft.
Forfattere
Anne Loft1, Isabel Forss1*, Majken Storm Siersbæk1*, Søren Fisker Schmidt1, Ann-Sofie Bøgh Larsen1, Jesper Grud Skat Madsen1, Didier Pisani4, Ronni Nielsen1, Mads Malik Aagaard1, Angela Mathison2, Matt J. Neville3, Raul Urrutia2, Fredrik Karpe3, Ez-Zoubir Amri4, Susanne Mandrup1
* Disse forfattere har bidraget lige meget.
Tilknytninger
1 Institut for Biokemi og Molekylær Biologi, Syddansk Universitet
2 Laboratory of Epigenetics and Chromatin Dynamics, Mayo Clinic, Rochester, MN 55905, USA
3 National Institute for Health Research, Oxford Biomedical Research Centre, Oxford, UK
4 Univ. Nice Sophia Antipolis, iBV, CNRS UMR 7277, INSERM U1091, 06100 Nice, France
Kontakt
Professor Susanne Mandrup
Tlf: +45 6550 2340
E-mail: s.mandrup@bmb.sdu.dk