
Ny indsigt i aggressiv brystkræft og potentielle behandlingsmuligheder
Patienter med triple-negativ brystkræft kan finde opmuntring i ny forskning fra professor Vijay Tiwari fra Institut for Molekylær Medicin.
Triple-Negative Breast Cancer (TNBC) er vanskelig at behandle på grund af sin aggressive natur og modstandsdygtighed over for kemoterapi. Men netop publiceret forskning fra Syddansk Universitet kaster lys over de mekanismer, der driver denne modstandsdygtighed og giver håb om bedre resultater for patienter i fremtiden.
To separate undersøgelser, udført af et team af forskere fra Institut for Molekylær Medicin, publiceret i tidsskrifterne Precision Oncology og EMBO Molecular Medicine, har dykket ned i forståelsen af resistens over for kemoterapi i TNBC og fundet nye veje til opdeling af patienterne og bedre behandling ud fra det.
Hvad er en biomarkør?
En biomarkør, også kendt som en biologisk markør, refererer til et målbart tegn på en biologisk tilstand.
Biomarkører findes oftest i prøver af blødt, urin eller væv og bruges til at undersøge typiske biologiske funktioner, sygdomsprocesser eller kroppens reaktion på medicinske behandlinger.
Professor Vijay Tiwari, leder af forskergruppen, siger:
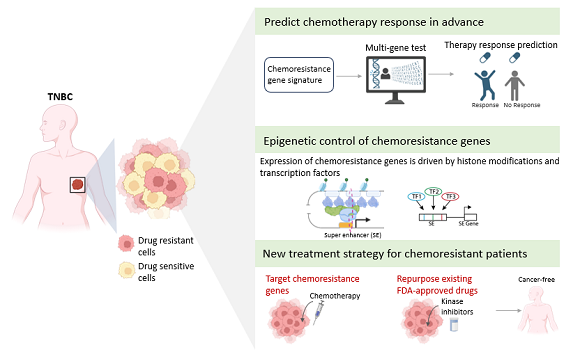
-Vores resultater har identificeret specifikke grupper af celler i tumoren, der driver resistens over for kemoterapi, og yderligere afkodet det underliggende molekylære program, der er skyld i denne adfærd. Det betyder at vi i generne vil forudsige patienters respons på kemoterapi ved brug af eksisterende godkendte lægemidler. Det er en virkelig spændende udvikling med potentiale til væsentligt at forbedre livet for TNBC-patienter.
Særlige resistente celler
I den første undersøgelse brugte forskerne avancerede analyseteknikker til at afdække hidtil ukendte typer af celler i TNBC-tumorer. Det er netop disse celler, der viser tegn på resistens overfor kemoterapi. Forskerne fandt desuden frem til de gener, der giver cellerne denne modstandsdygtighed.
Postdoc Mohammed Inayatullah, hovedforfatter på denne undersøgelse, har i studiet brugt avancerede genomics-værktøjer kombineret med machine learning.
-Vi har opnået en øget forståelse af mekanismerne bag lægemiddelresistens, og kan med de her metoder potentielt finde frem til de bedste biomarkører til at udvikle behandling for de vanskeligste kræftformer, blandt andet TNBC, siger han.
Studiet peger desuden på potentielle alternative behandlingsmuligheder for TNBC-patienter, der er resistente over for kemoterapi.
→ Find studiet via dette link
Epigenetisk kontrol af resistens
Det andet studie, ledet af ph.d.-studerende Ryan Lusby, fokuserede på at udfolde de epigenetiske mekanismer, der driver kemoresistens i TNBC. Ved hjælp af data fra patienter med TNBC har forfatterne belyst, hvordan en specifik kemisk ændring på histonproteiner kontrollerede gener for kemoresistens.
Hvad er epigenetik og histonproteiner?
Epigenetik handler om at undersøge, hvordan adfærd og miljøfaktorer medfører ændringer, der påvirker genfunktionalitet.
I modsætning til genetiske ændringer er epigenetiske ændringer reversible og ændrer ikke DNA-sekvensen; dog kan de påvirke kroppens fortolkning af en DNA-sekvens.
Histonproteiner er vitale komponenter, der tilbyder strukturel forstærkning til kromosomer. Inden i hvert kromosom ligger et omfattende DNA-molekyle, der kræver indkvartering inden for cellekernen. Denne indkvartering lettes af DNA, der vikles omkring klynger af histonproteiner, og dermed bliver kromosomets struktur mere kompakt.
-Ved omfattende kortlægning af denne ændring hos TNBC-patienter fandt vi i vores studie nogle såkaldte superforstærkere, der driver udtrykket af gener, der er afgørende for resistens mod kemoterapi, siger Ryan Lusby.
-Bemærkelsesværdigt er især, at tab af transkriptionsfaktorer, der besætter disse superforstærkere, overvandt resistens.
Dette studie har afsløret, hvordan målretning mod genetiske og epigenetiske mekanismer, der ligger til grund for kemoresistens, tilbyder nye veje til terapi.
→ Find studiet via dette link
Mød forskeren
Vijay Tiwari. Professor og forskningsleder for Genombiologi ved Institut for Molekylær Medicin.